Dividido en 5 pasos, uno por cada bloque
I. VALOR SOCIAL Y JUSTIFICACIÓN
II. CUALIFICACIÓN DEL EQUIPO INVESTIGADOR
III. VALIDEZ CIENTÍFICA Y METODOLÓGICA
IV. ASPECTOS ÉTICOS ESPECÍFICOS
V. CUMPLIMIENTO DE LA DOCUMENTACIÓN
Para pasar de bloque hay que introducir todos los datos obligatorios del anterior y guardar.
Todos los apartados son obligatorios rellenarlos a no ser que este desactivado. Hay apartados que se activan si se responde que Sí a apartados anteriores.
I. VALOR SOCIAL Y JUSTIFICACIÓN
1.1 Valor social del proyecto
Viene de Datos generales el campo "Valor social" que un campo de text area, es de solo lectura
La parte:
"10.Otra finalidad. Especificar
Campo valor social del proyecto"
Sería lo que han introducir en el campo "otroValorSocial" de la tabla PeticionEvaluacion.
1.2 Justificación del uso de seres humanos
II. CUALIFICACIÓN DEL EQUIPO INVESTIGADOR
2.1 Personal que llevará a cabo las tareas con seres humanos, sus muestras y/o sus datos
Tabla con las siguientes columnas (viene informado por el equipo de investigación, es de solo lectura):
- Nombre
- NIF
- Vinculación
- Nivel académico
- Tarea
- Experiencia
III. VALIDEZ CIENTÍFICA Y METODOLÓGICA
3.1 Objetivos científicos del proyecto
Viene de datos generales, es de solo lectura
3.2 Diseño metodológico del proyecto
Viene de datos generales, es de solo lectura
3.3 Referencias de publicaciones científicas
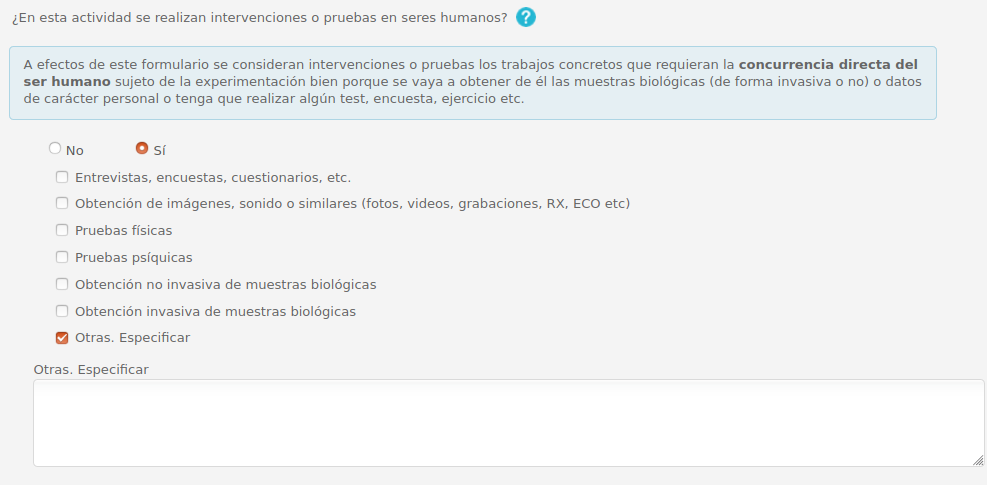
3.4 Intervenciones o pruebas en seres humanos
- 4.1.1 Tipo de riesgos o molestias
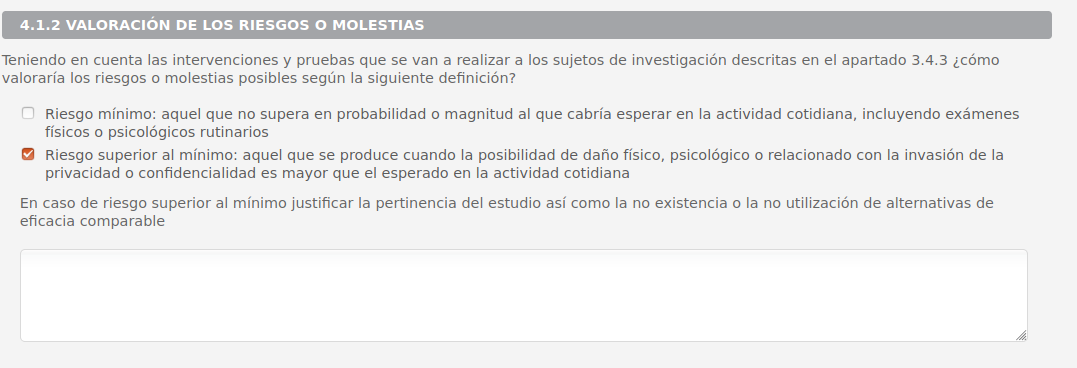
- 4.1.2 Valoración de los riesgos o molestias
CAmbiar texto
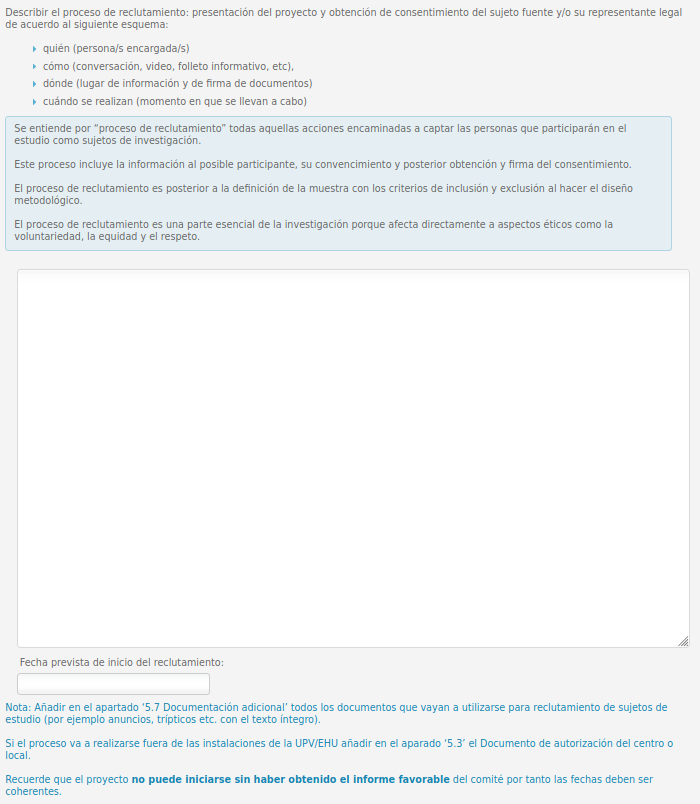
En la NOTA: donde pone UPV/EHU sustituirlo por UMU
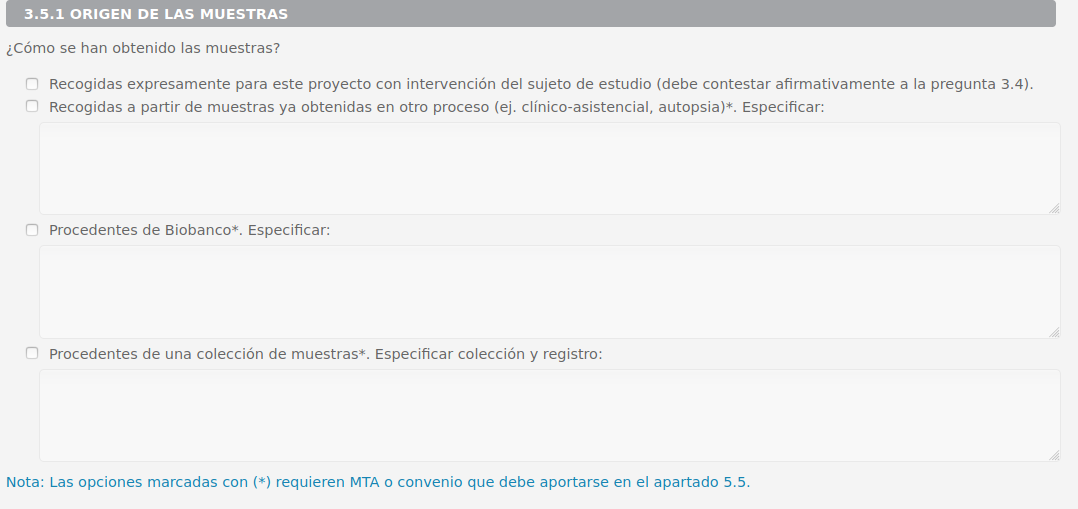
3.5 Muestras biológicas de origen humano CAmbiar texto
En la Nota dejarlo como se indica:
"Nota: Recuerde que la manipulación de tejidos/sangre/fluidos humanos requiere de evaluación del CEIAB CBE.
Las opciones marcadas con asterisco requieren el informe previo favorable de la Comisión de Garantías que debe aportarse en el apartado 5.5. Para más información sobre investigación con este tipo de muestras consultar el artículo 35 de la LIB 14/2007 antes de su utilización"
3.5.1
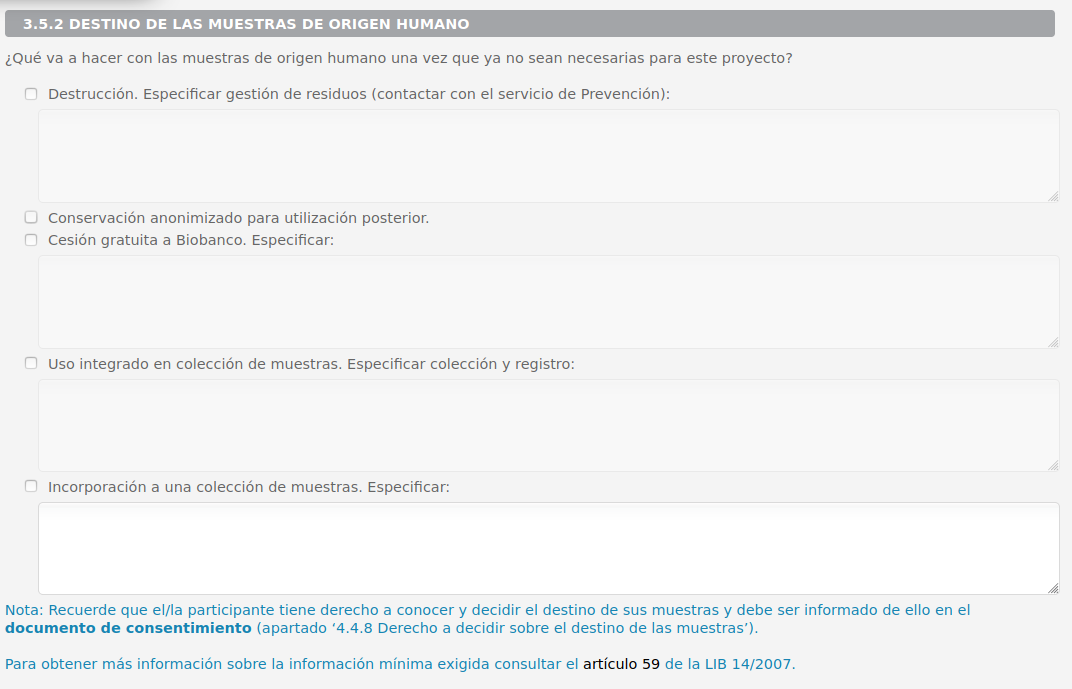
3.5.2
3.6 Datos de carácter personal PENDIENTE DE QUE NOS DIGAN LOS CAMBIOS
La caja de texto se activa si se contesta que "Sí"
IV. ASPECTOS ÉTICOS ESPECÍFICOS
4.1 Ponderación de los riesgos o molestias PENDIENTE ENLACE
"Para más información sobre el balance riesgo/beneficio consultar el documento de la CIOMS 'Pautas éticas internacionales para la investigación biomédica en seres humanos'"
4.1.1 Tipo de riesgos o molestias CAmbiar texto y PENDIENTE ENLACES
En la frase de la ayuda:
"Para obtener más información sobre la información mínima exigida consultar el artículo 15 de la LIB 14/2007 o la Guía para elaboración de documentos elaborada por el CEISH CEI."
4.1.2 Valoración de los riesgos o molestias
Si se selecciona "Riesgo superior...." se activa la caja de texto y el siguiente apartado 4.1.3 Minimización del riesgo o molestias superiores al mínimo
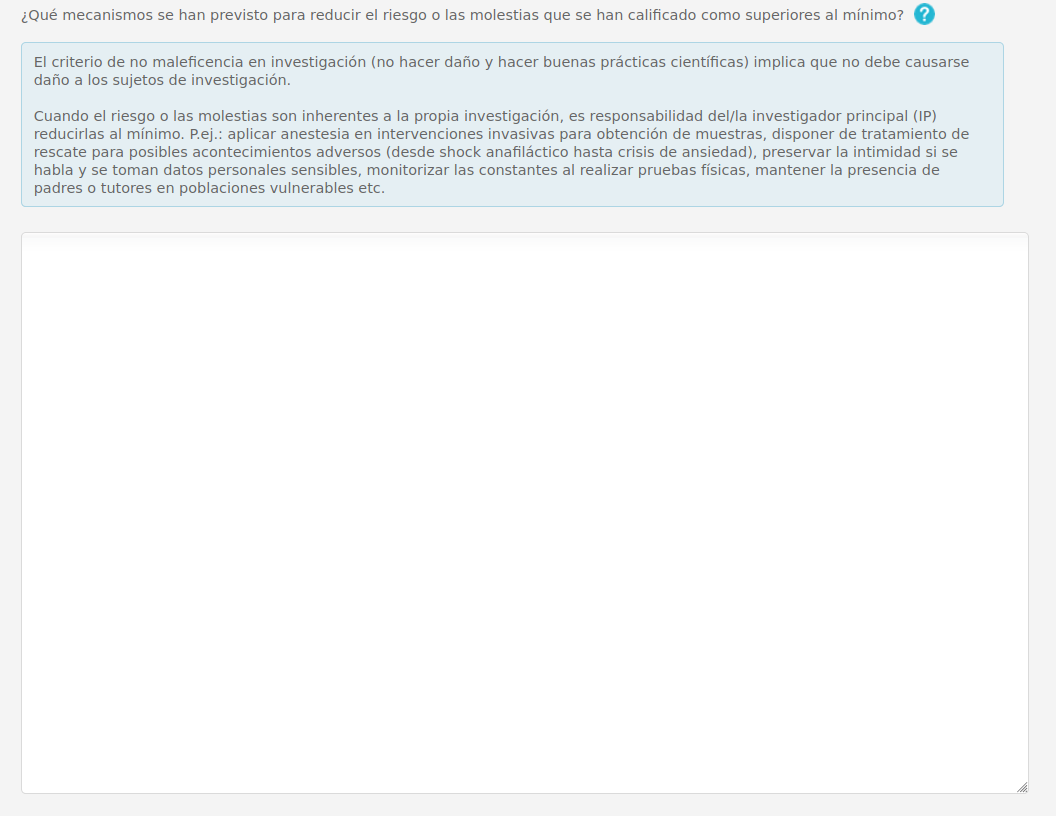
4.1.3 Minimización del riesgo o molestias superiores al mínimo
4.1.4 Aseguramiento del daño CAmbiar texto Y PENDIENTE
Sustituir en la ayuda UPV/EHU por UMU
Si se contesta que "Sí" se activa la caja de texto
4.2 Selección equitativa de la muestra CAmbiar texto y pendiente enlaces
"Para más información sobre la selección equitativa de la muestra consultar:
- Informe Belmont
Declaración Universal sobre Bioética y Derechos Humanos” (UNESCO)
- Documento de la CIOMS 'Pautas éticas internacionales para la investigación biomédica en seres humanos' (pauta 12)"
4.3 Protección de grupos vulnerables CAmbiar texto Y PENDIENTE ENLACE
Cambiar el título del apartado 4.3 PROTECCIÓN DE GRUPOS ESPECIALMENTE VULNERABLES
y los siguientes textos:
"¿Se trata de personas especialmente vulnerables? (menores, personas legalmente incapacitadas, etc.)
Son personas especialmente vulnerables aquellas que de forma absoluta o relativa no pueden proteger sus propios intereses. Se considera que esta capacidad se ve alterada cuando se da alguna de estas circunstancias:
- Está limitada su autonomía o autogestión por agentes internos (ej.menores, algunas enfermedades psíquicas graves, etc), o externos (personas institucionalizadas, relaciones de subordinación, recepción de subsidios, etc)
- Son precisas medidas específicas para garantizar su acceso a participar en proyectos de investigación en condiciones de igualdad y no discriminación (ej. personas en riesgo de exclusión, con alguna discapacidad, etc)
Para más información sobre grupos especialmente vulnerables y sus implicaciones éticas consultar el documento de la CIOMS Pautas éticas internacionales para la investigación biomédica en seres humanos (pautas 13 y sig)"
Especificar colectivos de personas especialmente vulnerables
Justificar por qué no se plantea la utilización de personas menos vulnerables
Especificar en qué pueden beneficiar los resultados de estas investigaciones a estas personas o colectivos especialmente vulnerables
Nota: recuerde que la condición especial de estas personas debe tenerse en cuenta y obliga a:
- Cuidar al máximo cuestiones como la voluntariedad, información, consentimiento, proceso de reclutamiento, etc. (ver apartados 3.4.1, 4.1 y 4.2) aquél que tenga la custodia
- En caso de menores de 12 años debe incluirse la firma de ambos progenitores en el documento de consentimiento, entre 12 y 18 años ha de incorporarse el asentimiento del menor, y en personas legalmente incapacitadas, debe incluirse la firma de su representante legal (ver punto 4.4.2 Información obligatoria mínima)
Para más información sobre protección de grupos vulnerables consultar los artículos 20, 21 de la LIB 14/2007.
Si se selecciona que "Sí" se activan las 3 cajas de texto siguientes.
4.4 Información y consentimiento CAmbiar texto y PENDIENTE ENLACE
Modificar CEISH por CEI
"Guía para elaboración de documentos (pdf), elaborada por el CEISH CEI."
Si se selecciona "No" se desactivan los apartados siguientes 4.4.1 Tipo de consentimiento y 4.4.2 Información obligatoria mínima
Si selecciona "Otros" se activa la caja de texto.
Si se selecciona "Sí" se activa los apartados siguientes 4.4.1 Tipo de consentimiento y 4.4.2 Información obligatoria mínima y la caja de texto.
4.4.1 Tipo de consentimiento
4.4.2 Información obligatoria mínima CAmbiar texto y poner enlace
Cambiar texto UPV/EHU por UMU
En vez del fichero pdf poner el siguiente enlace con el texto:
Modelos de la Universidad de Murcia de Hoja de Información y de Consentimiento Informado (https://www.um.es/web/comision-etica-investigacion/comision-etica/ceic)
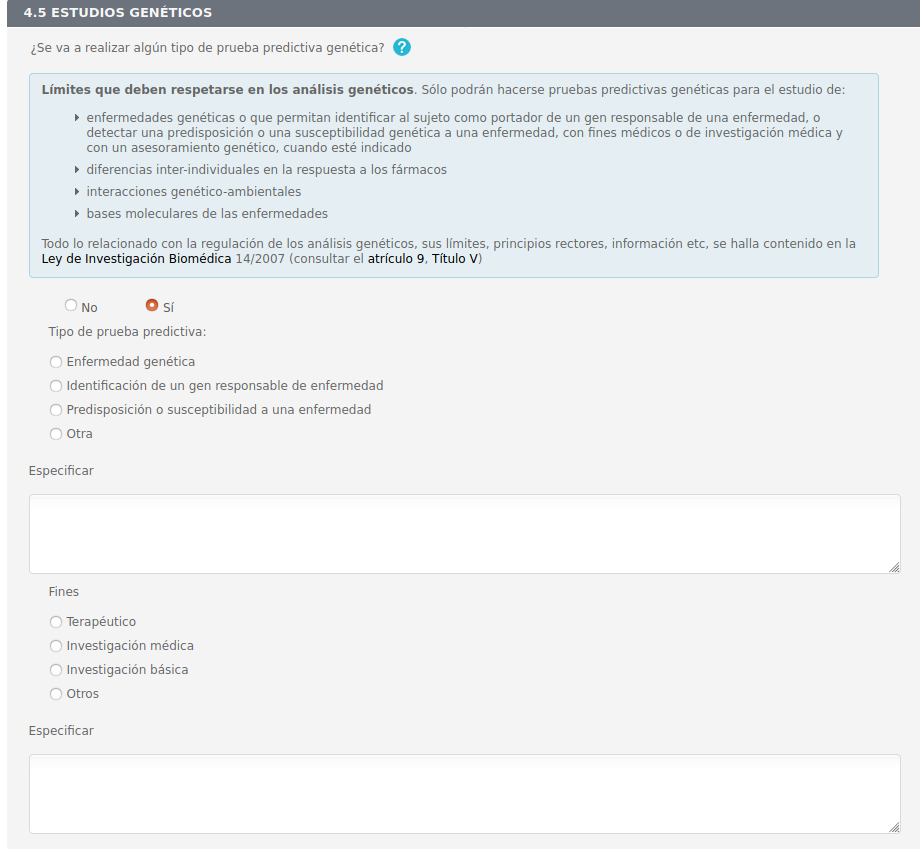
4.5 Estudios genéticos
Si se selecciona "No" todo el resto esta desactivado y también se desactivan los subapartados:
- 4.5.1 Resultado del estudio genético
- 4.5.2 Consejo genético
- 4.5.3 No discriminación por motivos genéticos
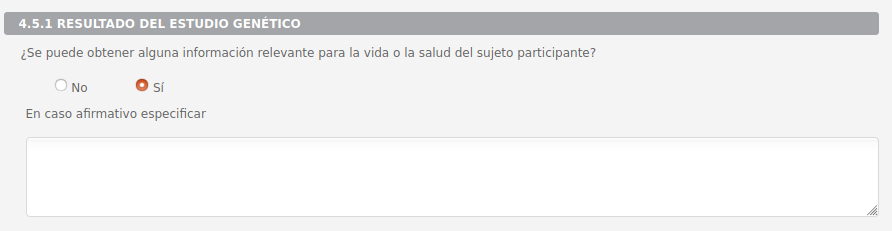
4.5.1 Resultado del estudio genético
Si se selecciona "Sí" se activa la caja de texto
4.5.2 Consejo genético
4.5.3 No discriminación por motivos genéticos
4.6 Estudiantes como sujetos de investigación CAmbiar texto
Sustituir en la pregunta "UPV/EHU" por "UMU"
Si se selecciona "No" todo el resto esta desactivado y también se desactivan los subapartados:
- 4.6.1 Justificación del uso de estudiantes
- 4.6.2 Beneficio formativo para el estudiante
- 4.6.3 Vinculación académica con el equipo investigador
- 4.6.4 Incentivos académicos
- 4.6.5 Uso de tiempo lectivo
- 4.6.6 Actividades alternativas
- 4.6.7 Protección de la privacidad
4.6.1 Justificación del uso de estudiantes CAmbiar texto
Sustituir en la pregunta "UPV/EHU" por "UMU"
Si se selecciona "No" hay que especificar los motivos, si se selecciona "Sí" se desactiva la caja de texto.
4.6.2 Beneficio formativo para el estudiante
Si se selecciona "Sí" se activa la caja de texto.
4.6.3 Vinculación académica con el equipo investigador pendiente enlace
4.6.4 Incentivos académicos
Si se selecciona "Sí" se activa la caja de texto.
4.6.5 Uso de tiempo lectivo
Si se selecciona "Sí" se activa la caja de texto.
4.6.6 Actividades alternativas
4.6.7 Protección de la privacidad
V. CUMPLIMIENTO DE LA DOCUMENTACIÓN
5.1 Documento de consentimiento
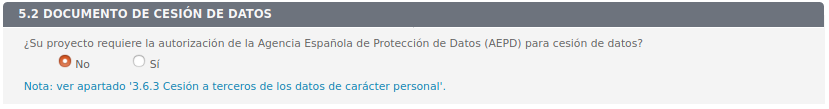
5.2 Documento de cesión de datos
5.3 Documento de autorización CAmbiar texto
Sustituir en la pregunta "UPV/EHU" por "Universidad" y en la ayuda
5.4 Documento de aceptación de colaboración
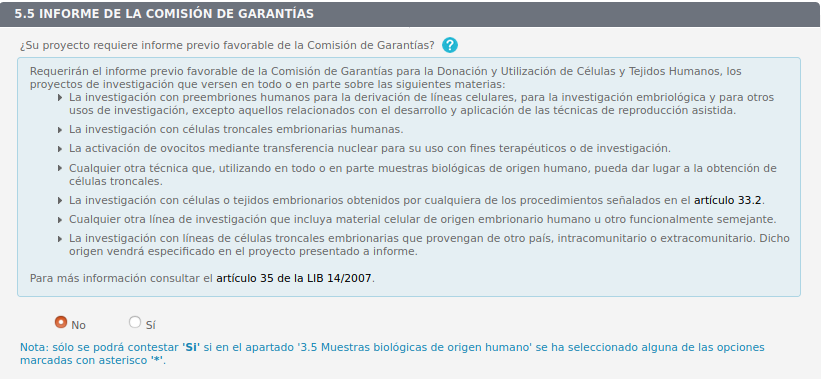
5.5 Informe de la Comisión de Garantías
Eliminar apartado
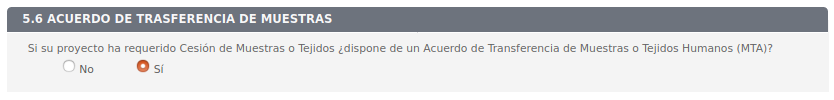
5.6 Acuerdo de trasferencia de muestras
Cambiar el número de apartado de 5.6 a 5.5
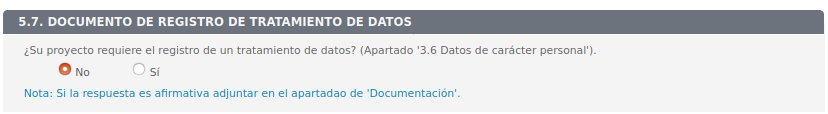
5.7. Documento de registro de tratamiento de datos
Eliminar apartado
5.8 Documentación adicional
Cambiar el número de apartado de 5.8 a 5.6
5.9 Aclaraciones al comité
Cambiar el número de apartado de 5.9 a 5.7